Home > 研究成果 > Zinc-finger antiviral protein mediates retinoic acid inducible gene I-like receptor-independent antiviral response to murine leukemia virus.
研究成果
齊藤達哉 (大阪大学免疫学フロンティア研究センター)
Lee H, Komano J, Saitoh Y, Yamaoka S, Kozaki T, Misawa T, Takahama M, Satoh T, Takeuchi O, Yamamoto N, Matsuura Y, Saitoh T*, Akira S*.
(*Co-corresponding authors)
Zinc-finger antiviral protein mediates retinoic acid inducible gene I-like receptor-independent antiviral response to murine leukemia virus.
Proc Natl Acad Sci U S A. 2013, 110, 12379-12384.PubMed]
Zinc-finger antiviral proteinは細胞内に侵入したレトロウイルスに対する感染防御応答を担う新たなタイプのパターン認識受容体である
私たちの細胞は、病原体に対するセンサーとして働くパターン認識受容体により、細胞内に侵入したRNAウイルスの特徴的なRNA構造を感知して、その排除を行います。このパターン認識受容体を介する感染防御応答は、自然免疫と呼ばれています。これまでの研究から、細胞内に侵入したインフルエンザウイルスやC型肝炎ウイルスなどのRNAウイルスに対する感染防御応答には、パターン認識受容体RIG-I-like receptors (RLRs)がI型インターフェロン(IFN)の産生を介して重要な役割を果たすことが明らかになっています。その一方で、細胞内に侵入したレトロウイルスに対するパターン認識受容体に関しては、不明な点が多く残されていました。私たちは、Zinc-finger antiviral proteinがレトロウイルスのRNAを感知し、RNA顆粒におけるエキソソームを介したウイルスRNA分解を誘導することを見出したので、ここに報告します。
マウス白血病ウイルス(MLV)は、マウスなどのげっ歯類に感染した際に、腫瘍形成を引き起こすレトロウイルスです。細胞外部(エンドソーム内)のMLVに対しては、一本鎖RNAを感知するパターン認識受容体であるToll-like receptor 7がウイルスRNAを認識して感染防御応答を誘導することが、近年の解析から明らかになっています。一方で、細胞内に侵入したMLVのRNAを感知してその排除を行うパターン認識受容体に関しては、不明な点が多く残されていました。
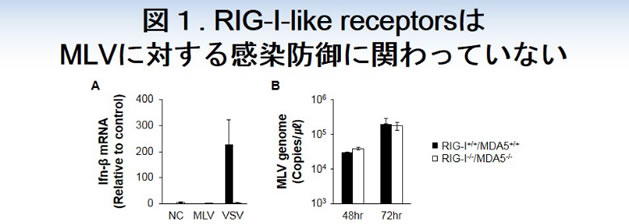
私たちはまず、様々なRNAウイルスに対する感染防御応答に関わるRLRsが、MLVに対する感染防御応答において果たす役割を解析しました。意外なことに、インフルエンザウイルスなどのRNAウイルスとは異なり、MLVはI型IFNの産生を誘導せず、RLRsによる感染防御応答から逃れていることが明らかになりました(図1)。
そこで私たちは、過剰発現によりMLVのRNAの分解を誘導することが知られていたZinc finger Antiviral Protein (ZAP)に関する研究を始めました。ZAPに関しては、内在性のZAPがMLVの複製を抑制することが出来るのか、ZAPによるMLVのRNAの分解が細胞質内のどのような場所で起こっているのかなど、不明な点が多く残されていました。今回の研究は、細胞質内に侵入したMLVに対するZAPを介した感染防御応答の空間制御のメカニズムを明らかにするものとなりました。
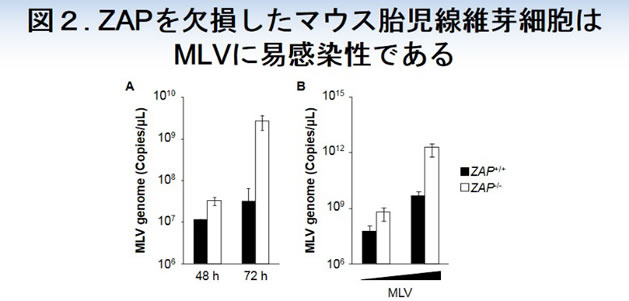
ZAPを欠損したマウス繊維芽細胞においてはMLVの増殖が大きく亢進することから、MLVに対する感染防御応答においてZAPが重要な役割を果たすことが明らかになりました(図2)。
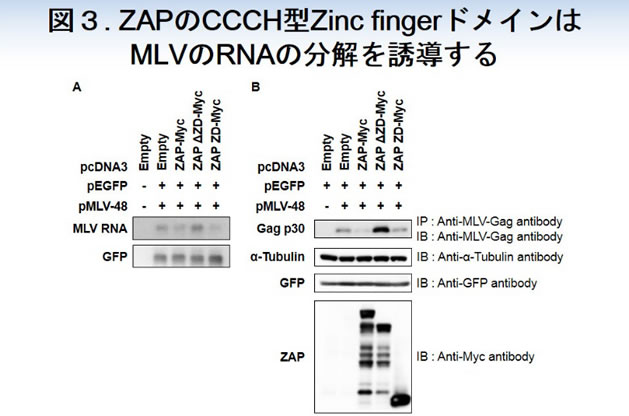
ZAPは、N末端側のCCCH型Zinc fingerドメインとC末側のPARPドメインを有しています。これらのドメインのうち、CCCH型Zinc fingerドメインがMLVのRNA分解に関与していることが明らかになりました(図3)。
続いて、ZAPの細胞内局在に関する解析を進めました。解析の結果、ZAPはCCCH型Zinc fingerドメインを介してP-bodyやストレス顆粒のマーカータンパク質が集まるRNA顆粒に局在することが明らかになりました(図4)。
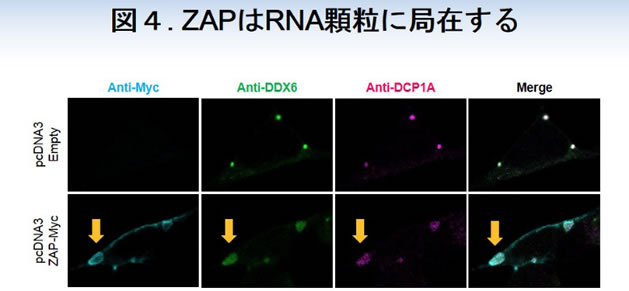
さらに、MLVのRNAの細胞内局在に関して解析を進めました。解析の結果、ZAPはCCCH型Zinc fingerドメインを介してMLVのRNAのRNA顆粒への局在を促進していることが明らかになりました(図5)。
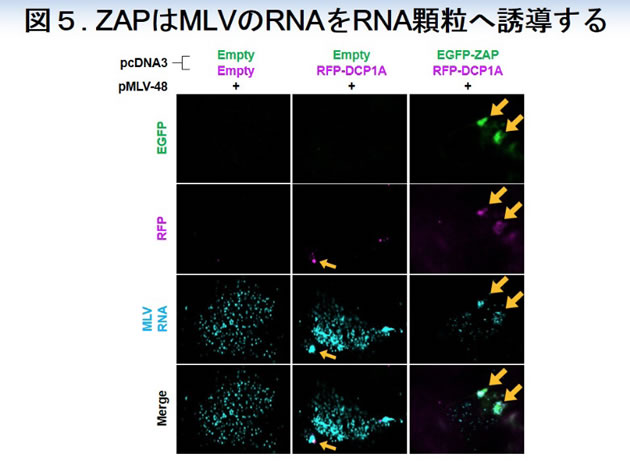
ZAPは、RNA分解機構であるエキソソームによりウイルスRNAの分解を誘導します。そこで、エキソソームの構成因子EXOSC5に関する解析を進めました。EXOSC5は、ZAPの発現によりRNA顆粒に局在するようになることが分かりました(図6)。
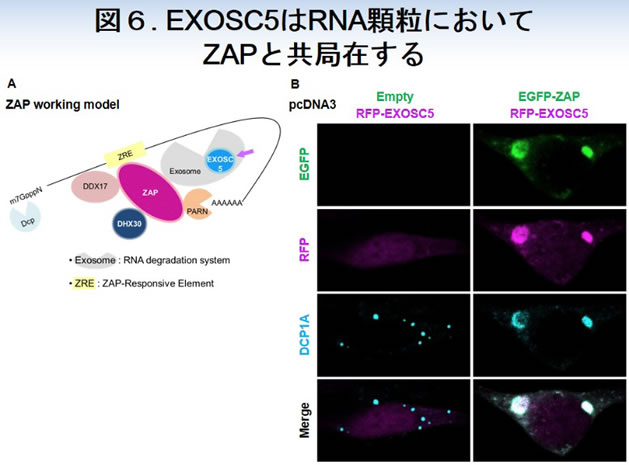
ZAPは、不死化したヒト上皮細胞においてRIG-Iを介したI型IFNの産生に関わることが報告されています。しかしながら、マウスのプライマリー胎児線維芽細胞や樹状細胞において、ZAPはRIG-Iを介したI型IFNの産生には関わっていませんでした(図7)。よって、ZAPによるMLVの排除にはRLRsは関与しないと考えられます。
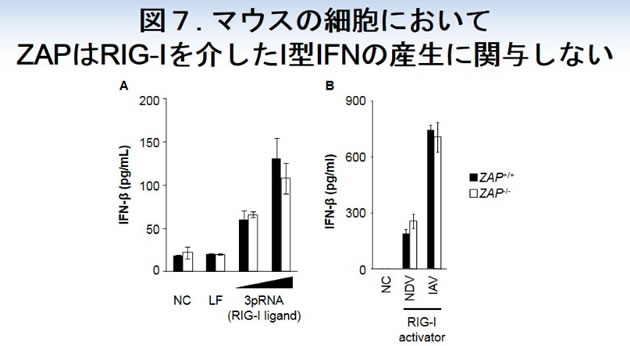
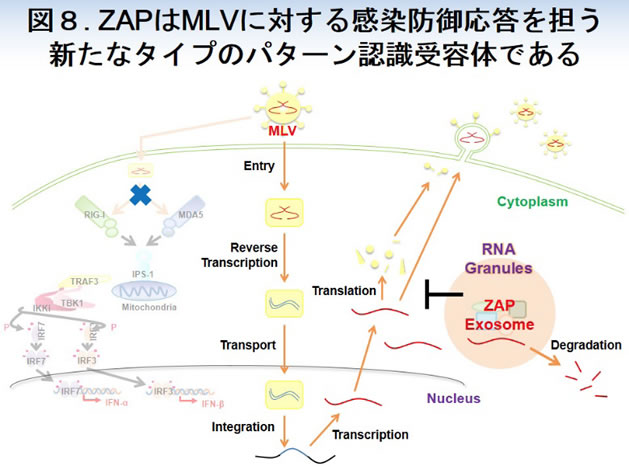
以上のことから、ZAPは細胞質内に侵入したRNAウイルスを感知してその排除を行う新たなタイプのパターン認識受容体であることが明らかになりました(図8)。