
Home > トピックス・イベント > 細胞内シグナル伝達の A-Cellモデル構築ガイド > 初級
細胞内シグナル伝達のA-Cellモデル構築ガイド 初級
|はじめに|基礎| 初級| 中級 | 上級| 初級 解説文PDF|
- 【初級】EGFRにおけるリガンドとレセプターの反応
- 【初級】視細胞桿体におけるシグナル伝達
- 【初級】膜型細胞外マトリクス分解酵素(MT1-MMP)による細胞外マトリクス(ECM)の分解
- 【初級】簡単な反応拡散:細胞外からのCa2+流入とそのバッファリング
【初級】EGFRにおけるリガンドとレセプターの反応
概要:EGFレセプター(EGFR/ErbB1R)は上皮系や神経系など多くの細胞膜表面に存在し、増殖や成長の制御に関わる上皮成長因子(EGF)がEGFRに結合することでMAPK経路などの活性化を行う受容体型チロシンキナーゼである。EGFの結合によってEGFR二量体が安定化し、これによって細胞質側のC末領域にあるリン酸化サイトが相互にリン酸化されて下流へとシグナルが伝達される(図1)。
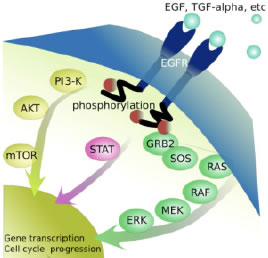
図1 EGFRシグナル伝達
ポンチ絵とA-Cellモデル:EGFRに関する数理モデル研究は多く行われており、論文の数も多い。SchoeberlらはEGFRの活性化から始まるMAPK経路のかなり詳細な数理モデルシミュレーションを行っており、ここではこの論文の中からEGFRの部分だけを抜き出して初級モデルとして数理モデルを紹介する。図2上はポンチ絵である。ここではEGFとEGFRが結合して複合体EGF・EGFRができること、それが二量体を形成することが示されている、両方向矢印で結合解離反応であることが表わされている。これをA-Cellでモデル化したものが図2中である。ほとんどポンチ絵と同じであるが、モデルの構造がよりはっきり示されている(A-Cellモデルはこちら)。
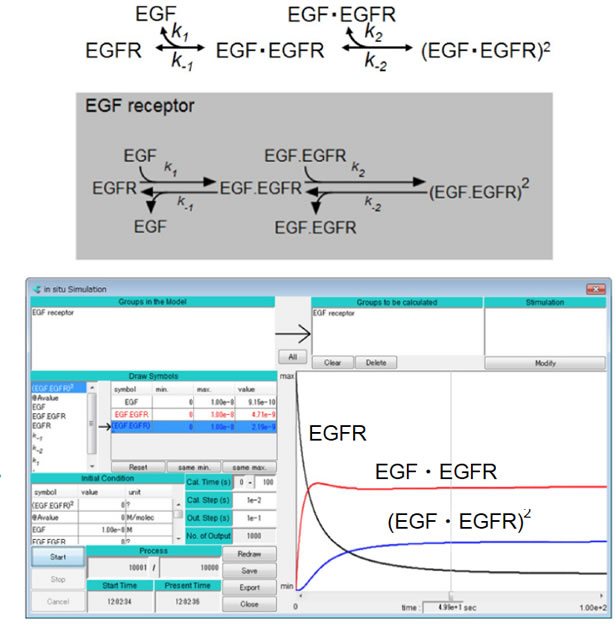
図2 EGFR活性化のポンチ絵(上)、A-Cellモデル(中)とシミュレーション結果(下)。
シミュレーション結果を図2下に示す。このシミュレーションではt=0から一定量のEGFが与えられ続け、それがEGFRと結合した場合の時間変化を示した。常に一定量のEGFが存在することをA-Cellで実現するためには、EGFのプロパティ画面のSymbol name下の4つのラジオボタンからconstを選択する。このとき様々なEGF濃度に対する(EGF・EGFR)2の平衡濃度をプロットすればdose-responseカーブを得ることができるので試してはいかがだろうか。
文献:Schoeberl, B., et al., Nat.Biotech., 2002, 370.
Hornberg, J.J., et al., Oncogene, 2005, 5533.
Klein, P., et al., PNAS, 2004, 929.
【初級】視細胞桿体におけるシグナル伝達
概要:網膜は外界からの光を受けて電気信号に変換して脳へ送るが、視細胞はその最初に位置する光信号→電気信号変換器である(図1)。
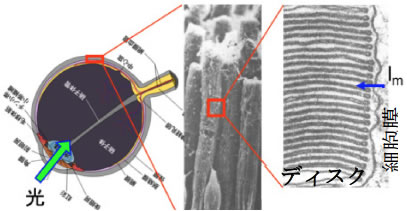
図1視細胞桿体の構造
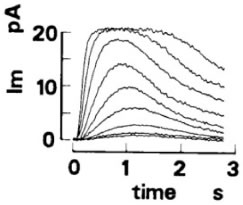
図2桿体の電流応答
光によって光受容体タンパク質ロドプシンが光異性化され、最終的には細胞膜にあるカチオンチャネルを閉じて、図2に示すような膜電流の変化(Im)が観測される。ロドプシンの光異性化から膜電流応答に至るシグナル伝達の概略は以下の通りである。
ロドプシン(Rh)→トランスデューシン(Gタンパク質)→PDE(cGMP分解酵素)→カチオンチャネル
ポンチ絵とA-Cellモデル:このシグナル伝達をもう少し詳しく描いたのが図3真ん中の楕円形(ディスク)とその周辺のポンチ絵である(上記青字で示した直線的シグナル伝達を①~④の番号で示している)。
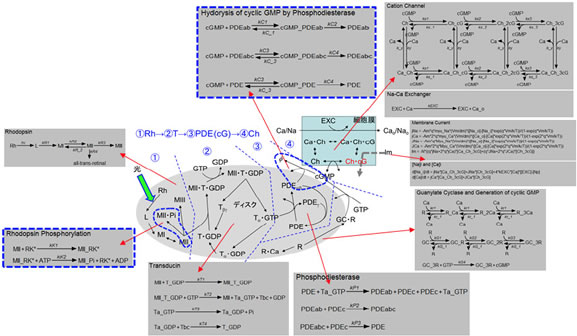
図3視細胞桿体におけるシグナル伝達のポンチ絵(中心付近の楕円形周辺)とそれに対応したA-Cellモデル(灰色の四角)。
ポンチ絵では反応の詳細までは詳しく記述していないが、A-Cellモデル(周辺の灰色四角枠)では詳しく表現してある。すなわち、まずタンパク質の反応の相互関係をポンチ絵で記述する。次に各反応が結合反応なのか、平衡反応なのか、酵素反応なのかなどによって、A-Cellが用意している7種類の反応アイコンの中から適切なものを選んでA-Cellモデルを作るわけである。なお図3のA-Cellモデルにはチャネルを流れる電流の式など、ポンチ絵には現れない部分も記述してある(A-Cellモデルはこちら)。
文献:Ichikawa, K., Neurosci.Res., Vol.19(1994), pp.201-212.
Ichikawa, K., Neurosci.Res., Vol.20(1994), pp.337-343.
Imai, H., et al., J.Biol.Chem., Vol.282(2007), pp.6677-6684.
【初級】膜型細胞外マトリクス分解酵素(MT1-MMP)による細胞外マトリクス(ECM)の分解
概要:細胞内で形成されたタンパク質が膜へ輸送され複合体を形成し、何らかの活動を行った後に細胞内へ取り込まれる。このようなタンパク質の動きをMembrane-type1matrix metalloproteinase(MT1-MMP, MMP14)を例にとってモデルを作成した。Fig.1に簡略化したMT1-MMPの動きを示した。MT1-MMPは細胞膜へ挿入後Tissue inhibitor of metalloprotease-2(TIMP2)とMatrix metalloproteinase-2(MMP2)の3分子によって多様な複合体を形成する。形成された複合体は細胞外マトリックス(ECM : extracellular matrix)の分解を行う。その後、MT1-MMP複合体は細胞内へ移行する。
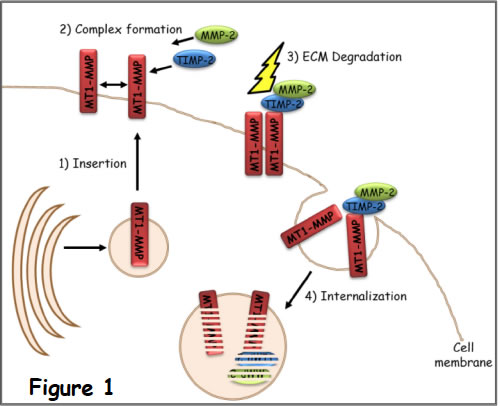
ポンチ絵とA-Cellモデル:MT1-MMPの挿入から細胞内移行までの流れは1)Insertion 2)Complex formation 3)ECM degradation 4)Internalizationの4つに分けられる。それぞれに対応するA-Cellモデル(こちら)とモデル作成時のポイントを以下にまとめた。
1) Insertion
MT1-MMP(Mid)はVesicleを介して細胞膜へと挿入される。
Vesicleが細胞膜へ挿入される際の膜融合にかかる時間がvesicle輸送の時間間隔に比べて無視できる程度であると考え、A-Cellのstimulationの中からデルタ関数を選択してMT1-MMPの挿入を構成する(Fig.2)。
Figure 2
2) Complex formation
| 膜に挿入されるタンパク質→MT1-MMP(MMP14) 複合体形成に使用される他のタンパク質→TIMP2, MMP2 |
以上の3分子から形成可能な複合体と複合体の形成経路を Fig.3に示した。形成される複合体は、それぞれが結合して新しい複合体を形成することから、Fig.3のような状態遷移図を描くことで、A-Cellモデル(Fig.4)を構築する時に複合体とその形成経路の欠損や重複を避けることが可能になる。
Fig.3で形成される複合体の中の1つであるMMP14・MMP14・TIMP2・MMP2は複合体形成の後MMP2を活性化することが知られている。そこでFig.5の反応を加える(上段はactivation、下段はdeactivation)。
なおFig.3と4でECM分解を行うMT1-MMP複合体は4種類あり、M14、M14.M14、M14.M14.T2、M14.M14.T2.M2である。
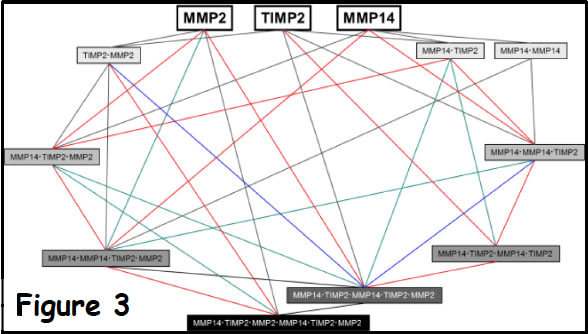
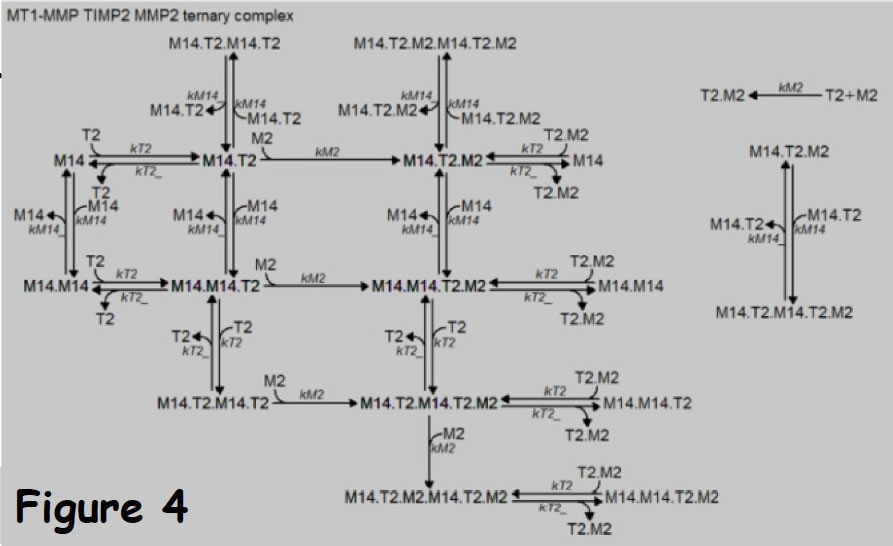
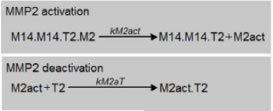
Figure 5
3) ECM degradation
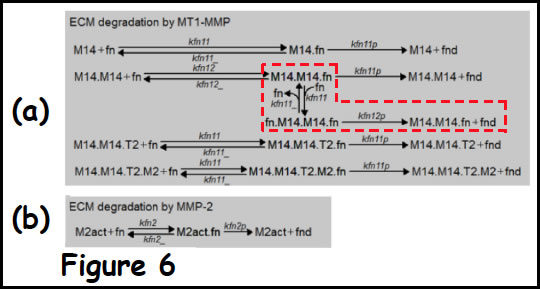
細胞膜上で形成されたECM分解能を有する複合体4種と複合体形成に伴って活性化されたMMP2(M2act)が行うECM分解をA-Cellモデルで表すとFig.6になる(ミハエリス・メンテン型反応式による)。Fig.6(a)はECM分解が可能な複合体4種類によるECMの分解を、(b)はM2actによるECM分解を示している。ECM(ここでは実験を想定してfibronectin)は分解されてfndとなることでfibronectin(fn)が減少するようにモデルを作成した。M14.M14はECMとの結合サイトが2ヵ所あることから赤い破線で囲った反応を加えた。
4) Internalization
MT1-MMPの挿入(Fig.2)による膜上のMT1-MMPは、細胞内移行とバランスすることで膜上濃度を一定に保たなければならない(Fig.7)。ここではモデルの簡単化のため、MT1-MMPと複合体として細胞内移行したTIMP2とMMP2はInternalizeされた後も名称を変えていない。こうすることで、TIMP2やMMP2の分泌という新たなプロセスを導入することなくそれらの総濃度を一定に保つことができる。
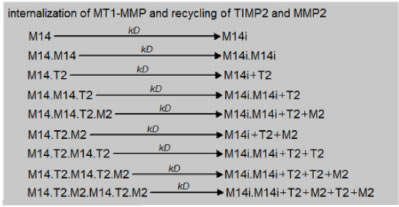
Figure 7
文献:Hoshino D., et al., PLos Comput Biol., Vol.8(2012), e1002479
【初級】簡単な反応拡散:細胞外からのCa2+流入とそのバッファリング
概要:カルシウムイオンCa2+は細胞のシグナル伝達や機能維持に重要であり、その濃度は厳密に制御されていて細胞内Ca2+濃度は細胞外に比べて4桁以上低い。細胞内のCa2+濃度の制御には細胞膜のCa2+透過性チャネルの開閉、細胞内でのERからの放出、Ca2+バッファによる制御などいくつもの要因があるが、ここでは細胞膜のCa2+透過性チャネルが開いたことによるCa2+流入とそのバッファリングについて例を示す(図1)。
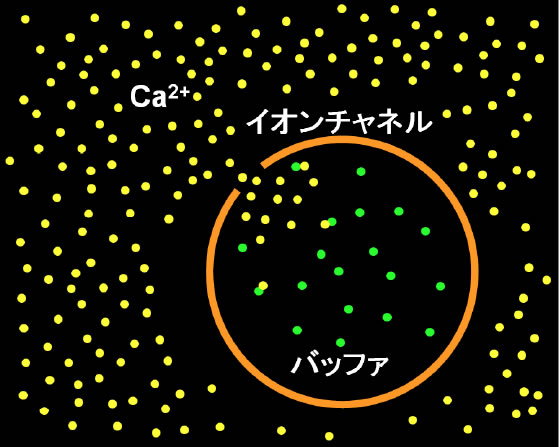
図1 Ca2+流入とバッファリングの模式図
ポンチ絵とA-Cellモデル:Ca2+とバッファとの結合解離反応についてポンチ絵を図2左に、そのA-Cellモデルを中に、円形形態モデルを右に示す。Ca2+流入は形態モデルの一番上の赤く示した5コンパートメントから生ずるとした。従ってSource刺激はこれらのコンパートメントにのみ、一方バッファリング反応は全体に割り付けた(A-Cellモデルはこちら)。
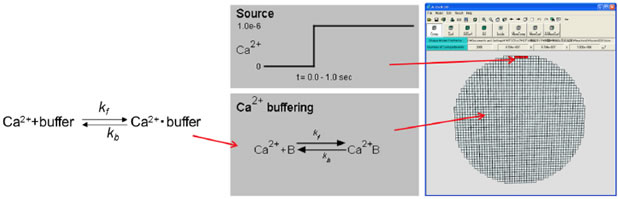
図2 ポンチ絵とA-Cellモデル
シミュレーション結果を図3に示す。このシミュレーションではt=0からCa2+が流入し、バッファ分子Bと反応しながら細胞内を拡散する。Ca2+拡散定数は10-10 m2/sである。
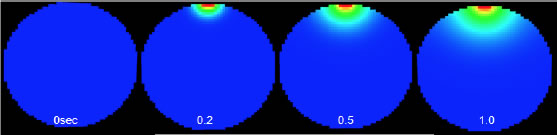
図3 シミュレーション結果
Bは拡散させていない。バッファ分子Bがない場合(湧き出しのある拡散)と比較してみてはいかがだろうか。











