αクロトーが認識する糖鎖の構造決定とシグナル様式の解明
 |
研究代表者 伊村明浩 先端医療振興財団 (協力研究者:前田良太) |
研究概要
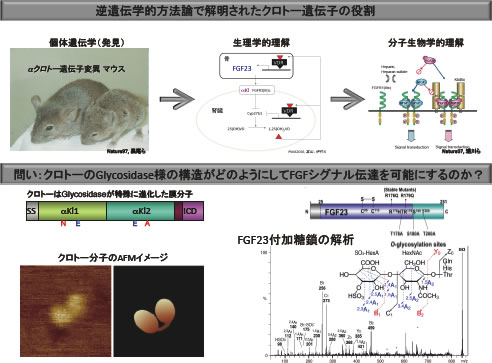
【背景】αクロトーは変異マウスの原因遺伝子として発見され、当初「老化関連遺伝子」と解釈された。しかしその後の研究により、αクロトー個体での役割は、PTH分泌制御とビタミンD抑制であり、ミネラル代謝の鍵分子である事が判明した。αクロトーは分子機能として、Na,K-ATPaseとFGF23への結合により、それぞれの活性制御を行う (Science07, PNAS10)(図参照)。この機構により、個体のミネラル恒常性維持を可能にする。しかし、どのようにして複数の分子に結合して活性調節することができるのかは不明であった。最近我々は、αクロトーはグルクロン酸を認識して結合する新タイプの特異的レクチンであることを突き止め、αクロトーの糖認識とシグナルの関連性に焦点を当てて解析している。
【目的】αクロトーがどのようにしてFGF23やNa,K-ATPaseに結合し、特にFGF23シグナルにおける結合様式と病理学的役割を解明する
【研究方法】最近我々は、BIAcoreを用いた結合解離解析、MSによる糖鎖解析によって、αクロトーが認識するFGF23のo-結合型修飾糖鎖の末端がグルクロン酸であることを突き止めた。さらに、末端グルクロン酸には硫酸基が結合していることがMSスペクトルによって予想された。この事実は、硫酸化グルクロン酸を認識するHNK-1抗体によっても支持された。硫酸化グルクロン酸は、ヘパリンおよびヘパラン硫酸が有する構造で、生体内では広く存在するが、o-結合型糖鎖末端としては報告例がない。従って本研究は、グルクロン酸の何位に硫酸基が付加されているかという問題を解決するために、MS以外で構造を確定できる手法を援用することにより構造決定する。加えて、硫酸化グルクロン酸の標品化合物を作成し、αクロトーとFGF23の結合を競合阻害することを証明し、構造を確認する予定である。また我々は、エストロングルクロン酸(EG)がαクロトーに結合して阻害作用を有することを発見しているので(JBC04)、これを硫酸化した化合物(硫酸化EG)をモチーフとする化合物を作成し、生体内とくに腎臓と副甲状腺でも阻害的に働くかどうか検証する。本研究は、糖認識配列を有する受容体αクロトーが、新規の糖鎖構造にアクセスすることで生体内活性を決定しているという概念を提示し、未知の修飾シグナル様式を理解した上で、このシグナルがベースであると考えられる、腎不全におけるミネラル代謝病態の治療に寄与する事を目指している。
【参考文献】
- Tomiyama K, Maeda R, Urakawa I, Yamazaki Y, Tanaka T, Ito S,
Nabeshima Y, Tomita T, Odori S, Hosoda K, Nakao K, Imura A, Nabeshima Y.
Relevant use of Klotho in FGF19 subfamily signaling system in vivo.
Proc Natl Acad Sci U S A. 2010 Jan 26;107(4):1666-71. - Yamazaki Y, Imura
A, Urakawa I,
Shimada T, Murakami J, Aono Y, Hasegawa H, Yamashita T, Nakatani K, Saito Y,
Okamoto N, Kurumatani N, Namba N, Kitaoka T, Ozono K, Sakai T, Hataya H,
Ichikawa S, Imel EA, Econs MJ, Nabeshima Y.
Establishment of sandwich ELISA for soluble alpha-Klotho measurement: Age-dependent change of soluble alpha-Klotho levels in healthy subjects.
Biochem Biophys Res Commun. 2010 Jul 30;398(3):513-8. - Brownstein CA, Adler F, Nelson-Williams C, Iijima
J, Li P, Imura A, Nabeshima Y,
Reyes-Mugica M, Carpenter TO, Lifton RP.
A translocation causing increased alpha-klotho level results in hypophosphatemic rickets and hyperparathyroidism.
Proc. Natl. Acad. Sci. U S A. 105(9): p3455-p3460. (2008) - Nabeshima Y, Imura
A.
alpha-Klotho: a regulator that integrates calcium homeostasis.
Am. J. Nephrol. 28(3): p455-p464. (2008) - Imura A, Tsuji Y, Murata M,
Maeda R, et al.
alpha-Klotho as a regulator of calcium homeostasis.Science. 316(5831): p1615-p1618. (2007) - Sato A, Hirai T, Imura
A, Kita N, et al.
Morphological mechanism of the development of pulmonary emphysema in klotho mice.
Proc. Natl. Acad. Sci. U S A. 104(7): p2361-p2365. (2007)